
7 Апреля 2021
МОСКВА, 7 апреля - Ученые из Сколтеха по-новому определили какое-то из фундаментальных химических понятий — электроотрицательность, и предложили свою шкалу для его оценки, которая отличается от классической шкалы Полинга. Статья опубликована в журнале Nature Communications.Электроотрицательность — квантитативная характеристика способности атома оттягивать к себе электроны других атомов. Это одно из важнейших понятий в химии, необходимое для объяснения многих свойств — от энергии химических связей и неизменности соединений до цвета и твердости кристаллов.
Современное понятие об электроотрицательности акцепторов было введено американским химиком, нобелевским лауреатом Линусом Полингом в 1930-х годах. Он же предложил первую шкалу относительных атомных электроотрицательностей, основанную на косточки атома притягивать электронную плотность. В химической связи более электроотрицательный атом получает дополнительные электроны, становясь отрицательно заряженными, в то время как менее электроотрицательный атом теряет электроны и есть положительно заряженным.
Шкала Полинга наполняет значения от 0, 7 для атомов франция до 4, 0 для атомов фтора. Фтор — наиболее электроотрицательный элемент, за ним следует кислород со значением 3, 5, потом азот, хлор и так далее.
Полинг вывел свои значения электроотрицательности из термохимии, используя энергии некоторых химических связей. Он предложил простейшую формулу для расчета стабилизации связи из-за недостающая суммы в электроотрицательности между атомами. Однако со временем стало толкового, что формула Полинга дает довольно низкую точность.
Поэтому различные ученые в разное время предлагали свои определения электроотрицательности, которые грубо можно разделить на спектроскопические — для изолированных атомов — и термохимические — характеризующие энергии связи и теплоты образования соединений.
Российские хитрецы из Сколтеха профессор Артем Оганов и исследователь Кристиан Тантардини записали изменения в формулу Полинга и на ее основе создали новую термохимическую шкалу электроотрицательности.
Все возникло с того, что мы решили вычислить электроотрицательность Полинга под давлением, — приводятся в пресс-релизе Сколтеха слова Артема Оганова. — Химия высоких бремён довольно экзотична. Тем не менее, вы, возможно, сможете понять многое, как только узнаете, как электроотрицательность элементов изменяется под бременем. Мы использовали определение Полинга для расчета электроотрицательности в природных условиях и были поражены, обнаружив, что ее масштаб не соответствует ни теоретическим, ни экспериментальным энергиям связи. Более того, многие публикации в химической литературе упоминают об этом несоответствии, но ни одна не предлагает последовательного решения.
Я понял, что главная причина заключалась в том, что Полинг рассматривал ионную стабилизацию молекулы как аддитивный эффект. Если рассматривать ее как мультипликативный эффект, то многие недостатки будут устранены. С поддержкой новой формулы и экспериментально заполученных энергий химических связей мы пристроили электроотрицательность всех элементов и заполучили красивую шкалу, которая мучается как для малых, так и для больших разностях в электроотрицательности, — отмечает ученый.
В новой формуле, в различие от шкалы Полинга, электроотрицательность является безразмерной величиной и, по словам авторов, удобнее описывает химические связи, смелости молекул и реакции.
Редактор рубрики
Олег Кудрин
Место события на карте мира:

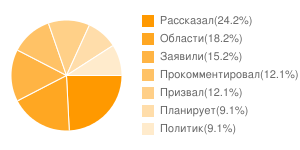
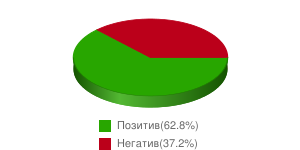 .
.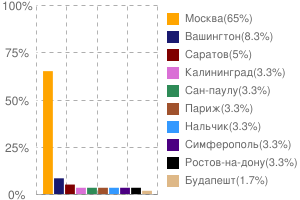 .
.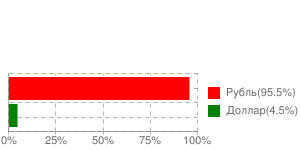 .
.
Комментарии к новостям
[17 Января 2024, 13:43] Александр Хомяков Замечательно! Не ожидал такой оперативности. Спасибо огромное! Всё работает и обновляется....
[15 Апреля 2022, 20:25] Ангелина Сметанина Скоро не только сократят, а много заводов вообще закроют и начнется бум китайских авто. Даже сейчас Эксид уже бешеные темпы по количеству проданных машин показывает...
[27 Декабря 2021, 21:44] Ева Воробьева Искренне рада за победителя! Но если бы мне так крупно повезло, то я прибежала бы за выигрышем в первый же день???? ...
[2 Сентября 2021, 13:11] Дмитрий Ершов Это хорошо. Значит клиенты долго ждать не будут. ...
[13 Мая 2021, 16:26] Олег Андреев "Мальдивы сутунки 65 государством, зарегистрировавшим расейскую вакцину против коронавируса Спутник V, сообщил Российский фонд секущих инвестиций (РФПИ)". Что это за йязыг?...
[2 Ноября 2020, 15:22] Лета Мирликийская риветсвую вас я с 6-ти лет пишу мне нужно все мои произведения задействовать в компьюторных программах образования по литературе и языкам и играм к примеру если ваши учащиеся напишут...
[20 Октября 2020, 09:22] Евгений Зимин Сузуки в этом году хорошо прибавили, уже не первый раз оба их пилота на подиуме. Видимо, для команды возвращаются "золотые" времена и есть шанс наконец оформить чемпионство после длительного перерыва....